2016年7月,爱康医疗基于3D ACT技术研发的脊柱椎间融合器正式获得了国家食品药品监督管理总局批准,这也是中国首例获得CFDA上市许可的金属3D打印椎间融合器产品。
该产品由北京大学第三医院骨科刘忠军教授团队和爱康医疗共同研发,历经七年研发和临床验证,终于完成了这个自主知识产权创新产品的上市注册审批。国械注准20163461289
产品原理
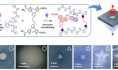
3D ACT技术是电子束熔融金属3D打印技术(EBM)、精准解剖结构三维重建技术、医工交互平台和三维设计平台等来自临床医学、计算机技术、材料学和机械设计多方面技术的融合体,相比传统的锻造、铸造、喷涂等技术,轻松实现钛合金植入物和表面类骨小梁结构的自由构建,体现了精准医疗和精准构建的先进科技理念,因此被命名为3D ACT(三维精准构建技术)。
3D ACT技术优势
1.类骨小梁结构优势
·达80%孔隙率
·800±μm孔径结构
·利于骨细胞的迁移和增殖
·汇集BMP及抗炎因子,有道骨愈合
2.类松质骨的弹性模量,避免应力遮挡及骨吸收,防止终板塌陷
3.良好的生物相容性和可靠地骨整合
4.微孔表面提供极佳的初始稳定性
3D ACT产品特点
1.充分的终板接触
·弧形表面,完全贴合终板穹隆
·宽度15mm,深度12.5mm
·楔形、弧形
2.6种高度,每1mm递增
·5-10mm
3.3种前凸角,符合多种矫形设计
·0°、4°、8°
5.预留植骨窗,满足植骨要求
适应症
与脊柱辅助内固定系统及移植骨匹配,适用于脊柱滑脱、椎间盘退变、椎管狭窄、假关节和脊柱不稳以及需要进行颈椎节段性融合的病变。
规格
用于ACDF手术
777 0
登陆后参与评论
2025-03-31 10:17:20

2025-03-12 10:26:43
2025-03-12 10:11:56

2025-03-11 10:00:32

2025-03-11 09:57:10

2025-03-11 09:53:04

2025-03-11 09:50:56

2025-03-11 09:45:00

2025-03-11 09:35:25

2025-03-10 11:00:08

2025-03-10 10:58:03

2025-03-10 10:57:16